
抗体药物是近来医药研究领域的热点。相比传统抗体,纳米抗体由于其分子量小,蛋白稳定性好,亲和力和特异性强,具有极好的研究、应用前景。
自然资源部第三海洋研究所海洋生物遗传资源重点实验室李增鹏课题组在海洋软骨鱼纳米抗体方面进行了多年的研究,构建了基于免疫、天然库、合成库、蛋白定向进化等纳米抗体研究平台,并取得了一系列科研成果。蛋白质靶向降解技术(TPD)如PROTAC在过去20年取得显著进展,新的基于溶酶体的TPD策略如LYTAC、ATTEC和AUTOTAC技术推动了该领域的发展。最近的研究发现关键蛋白在降解过程中形成“降解凝聚体”,其中p62小体是典型代表,可能通过减少空间距离实现有效降解。
2024年3月5日,清华大学生命学院李丕龙课题组和第三海洋研究所李增鹏课题组在Cell Research杂志合作发表了题为An all-in-one targeted protein degradation platform guided by degradation condensates-bridging bi-specific nanobodies的研究工作。这项研究突破性地利用了一种全新的蛋白质靶向降解技术,名为PDF-Bin。
该技术的核心创新在于发现并利用了一种双特异性纳米抗体,能够同时结合p62蛋白和靶标蛋白,从而将靶蛋白特异性地招募至p62降解凝聚体中,实现了高效的靶向降解。这种双特异性纳米抗体的应用,研究团队证明了PDF-Bin对于多种亚细胞定位和不同流动性的靶蛋白均具 有降解效果,展示了其广泛的应用潜力。
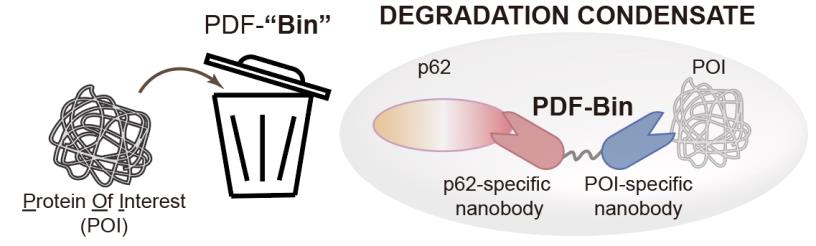
图1PDF-Bin示意图
此外,研究人员还发现PDF-Bin对于不同的靶蛋白选择了最优的降解途径,这一发现为蛋白质靶向降解技术的进一步优化和应用提供了重要启示。特别值得一提的是,该研究发现的双特异性纳米抗体相较于传统的小分子化合物具有更高的特异性和更强的结合力,从而降低了脱靶风险,为未来治疗药物的研发提供了更可靠的基础。
该研究为蛋白质靶向降解技术的发展和应用开辟了新的方向。该发现为解决难以成药的靶点提供了新的策略,并为未来的生物医药领域提供了新的研究方向。本文的通讯作者为清华大学生命科学学院李丕龙副教授和海洋三所“深海微生物创新团队”成员李增鹏研究员。清华大学生命科学学院2020级博士生贾雯为本文的第一作者,自然资源部第三海洋研究所2021级硕士生李伟杰在本研究工作中做出了重要贡献。
文章链接:https://www.nature.com/articles/s41422-024-00942-3
福建省厦门市思明区大学路184号
电话:86-592-2195608 传真:86-592-2195608
邮件:zhoujuan@tio.org.cn